結論:アナフィラキシーには直ちにアドレナリン、引き続きステロイドを使う
キーワード:喉頭浮腫、気道閉塞、マスト細胞、脱顆粒、β2受容体、耐性、グルカゴン
COVID-19(いわゆる新型コロナウイルス感染症)用のワクチンの接種が進められています。アナフィラキシーは、ワクチンの害反応として、まれとはいえ自発報告をもとにして100万回で5~20人[1]、医療従事者を対象にした日本の調査[1]を基にした厚生労働省(厚労省)の判断では65人、同じ調査を基にした本誌の検討で160人[2]、米国の医療従事者を対象にした綿密な調査では270人でした[3]。詳細な調査では4000人から6000人に1人という大変高頻度の発症となっています[3,4]。治療を間違えば命にかかわる重大な害反応です。世界人口(約70億人)の半分がワクチンを受けたとすると、約70万人がアナフィラキシーを起こすことになります。日本で、人口の半数6500万人が受けると1万人にアナフィラキシーが起こることになります。
アナフィラキシーを経験したことのある人の割合が、最近増えてきています。小~高校生でアナフィラキシーを経験したことのある児童・生徒の割合が、2004年には0.14%(約700人に1人)でしたが、2013年には0.48%(約200人に1人)と急増していました[4](図1)。食物アレルギー(2.6%→4.5%)やアレルギー性鼻炎(9.2→12.8%)も増えているなかで、特にアナフィラキシーの増加程度が著しいといえます。米国では成人も含めて1.6%がアナフィラキシーを経験しているとの報告もあり[5]、決してまれな反応ではありません。
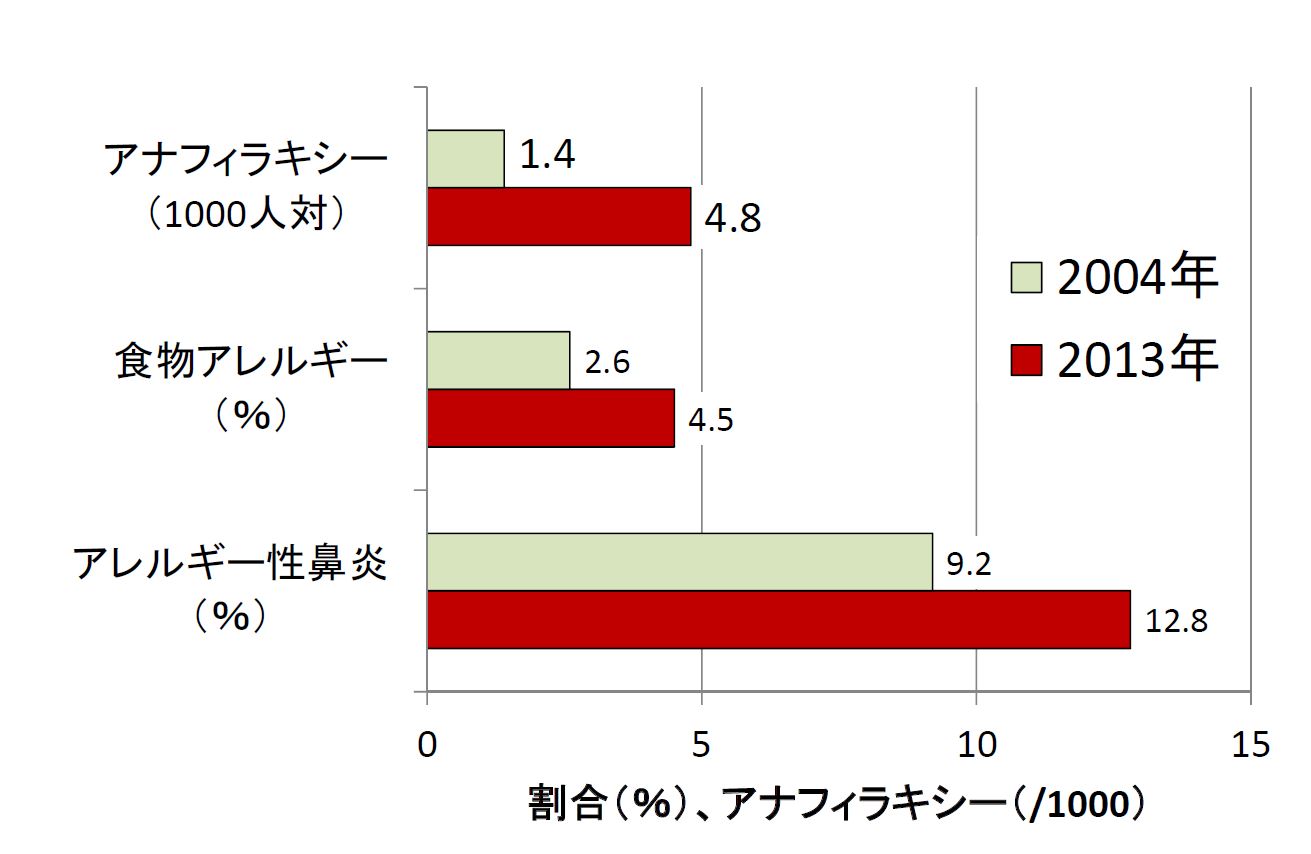
個々の薬剤や食物に対するアナフィラキシーは何万人に1人の頻度であっても、薬剤や食物は何千種類にも及ぶので、合計すると結構な頻度になるということでしょう。
このように、アナフィラキシーは、日常的に起こりうる薬剤による重大な害反応です。薬剤だけでなく、ソバアレルギーや蜂に刺されて起こるアナフィラキシーもあり[5-8]、適切な対処をしなければ、医療過誤事件にもなりかねません。死亡例では、起こりはじめから重篤であることもありますが、診断の遅れと、アドレナリン使用の遅れが大きく関係しています(後述)。
一方、1970年代にみられた誤った指針(ノルアドレナリンの推奨)は、最近の論説やガイドラインではさすがにみられなくなり、アドレナリンの使用が異口同音に推奨されています。これは適切です。
しかし、いくつかの点で、日本アレルギー学会のアナフィラキシーガイドライン[5]や重篤副作用疾患別対応マニュアル「アナフィラキシー」[6]それに世界アレルギー機関(World Allergy Organization: WAO)のガイドライン[7]には、不適切な記載が見られ、診断の遅れや、間違った治療が行われる可能性があります。本稿でこの機会に総点検しました。
アナフィラキシーの病態を理解し、速やかな診断と、適切な治療が行われ、救命可能なこの病態で、患者の命が失われることのないように願います。
アナフィラキシー(anaphylaxis)は、Portier とRichetが1902年にクラゲ毒の代わりにイソギンチャクの毒素で研究中に観察した現象につけられたものです。初回(0日目と3日目と2度)には何の反応も起こさなかった量を22日後に3度目に同じイヌに注射すると、数分後には喘ぎだし25分後に死亡したと報告されています[9]。この現象は、防御(phylaxis)に働かず、逆に重篤化したことから、「逆」を意味するanaをつけてanaphylaxis「アナフィラキシー」と命名されました。
その後、この反応は、1回目にイソギンチャクの毒素を接種されたイヌが感作されて起こるⅠ型アレルギーであることが判明しました[10]。アレルギーの4つの型のうちのⅠ型アレルギーは、1回目の接種で抗原に対するIgE抗体が体内にでき、これが2回目に接種された抗原と結合し、それがマスト細胞を刺激して反応を起こします。アナフィラキシーはI型アレルギーの中で最も重篤な反応です。
アナフィラキシーの重篤な症状は、基本的には、2つの仕組みで起こります。
アナフィラキシーは、I型アレルギー反応で起こることが多いのですが、それだけではありません(註1)。アレルギーを介することなく、化学的刺激や、アレルギーによらない薬物過敏(オピオイドやバンコマイシン、造影剤、消毒剤など)、さらには、寒冷や山での滑落事故による擦過傷など、物理的刺激でも起こります[5-8]。
原因のいかんを問わず、アナフィラキシーの症状は、基本的にマスト細胞が刺激されて放出された顆粒や、新たに作られる炎症誘発物質によるものです。そして、後で詳しく触れますが、このようなマスト細胞の活性化を抑えて、脱顆粒と炎症誘発物質の産生を止めることが、治療に直結するので、特に重要です(註1のアスピリン・NSAIDs喘息以外の機序は極めてまれな例外)。
アマスト細胞内にあらかじめ作られていた顆粒には、主にヒスタミンが含まれています。ヒスタミンは、激しいかゆみや浮腫を起こしますが、半減期は分単位[10]なので、新たな顆粒の放出を防ぐことができれば、比較的速やかに治まります。
一方、新たにマスト細胞内で作られる炎症誘発物質としては、ロイコトリエンDやプロスタグランジンがあります。これは5分から30分程度で出てきます。またTNFαやインターロイキン(IL)-4などサイトカイン類が、時間単位で作られます[10]。
マスト細胞は、体のあらゆる場所(粘膜下や結合組織)に分布していますが、臓器別の多さは人によって異なっています。アトピーで皮膚炎が出やすい人、花粉症で目にかゆみが起こりやすい人、鼻炎が起こりやすい人、気管支喘息の症状が出やすい人がいるのは、それぞれの臓器にマスト細胞が多くて反応しやすいからと考えると、理解しやすいでしょう。片頭痛もマスト細胞で起こりますが、これは頭や硬膜のマスト細胞が反応して炎症が起こるためです。
アナフィラキシーの症状も、人により強く出る部位が違います。これも、臓器別のマスト細胞の多さが関係しているでしょう。
アナフィラキシーの症状も蘇生時のA:airway、B:breathing、C:circulationの順で重要です[8](表1)。

最も重篤な症状は喉頭浮腫による気道(Airway)の閉塞です。喉頭部分(声帯のある部分)は狭いので腫れると気道が閉塞して、低酸素状態になり、意識消失やけいれん、ショックを起こします。この低酸素状態で起こるショックが最も重篤かつ危険で、死亡の最重要の原因となります。この状態では、患者は呼吸困難やゼーゼーといった呼吸症状を訴える間もなく呼吸が停止する [14,15] ので、経験のない医師には何が起こったのかわからないことがあります。
ジンマシンやかゆみ、発赤が出る間もない場合があります。この状態では、昇圧剤を使っても血圧は上がりません。アドレナリンを速やかに使い(できれば緩徐に静注し)、気管挿管して酸素補給が必要です。その後アドレナリンの持続点滴とステロイドが必要です。軽い症状は、声の変化(しわがれた声=嗄声)、のどが詰まる感じ、吸気性喘鳴(ヒーヒー)などです。
呼吸器症状:喉頭以外の気管支に主に作用すると気管支喘息のような、咳と喘鳴(ゼーゼー)、呼吸困難、頻呼吸、低酸素性のせん妄、チアノーゼが起こります。上記(A)のように、喘鳴もなくいきなり呼吸困難と呼吸停止の場合もあるので要注意。
血管の周辺で反応が起こり血管が拡張し、体液が血管外に滲みだし、血圧が低下し、頻脈になります。
ジンマシンやかゆみ、発赤が起こります。急激な例では、ジンマシンや発赤が起こる前に、口唇や手指先のシビレ、チカチカするといった症状で発症することもあります。
吐き気や腹痛、下痢、嘔吐といった症状になります。食べ物や内服薬剤でアナフィラキシーが起こるときには、まず、胃腸の粘膜が腫れて吐き気や腹痛が起こり、その後に下痢をし、次いでジンマシンが現れるといった順番で起こることがあります。
また、食べ物や内服薬剤の場合は、1回目は、こうした腹部の症状だけであったのが、2回目にはジンマシンまで出たけれど治まった。そして3回目に食べたり服用したりして、アナフィラキシーとなり、ショック状態となることがあります[13]。
(F)頭(脳、硬膜)にアナフィラキシーが起これば、頭痛やめまい、不安、突然の行動の変化、せん妄状態、あるいは重症例ではけいれんや意識障害になり、
(G)心臓にアナフィラキシーが起これば、不整脈が生じたり心筋虚血が生じたりします。
(H)その他:膀胱や、子宮など、あらゆる臓器でアナフィラキシーは起こりえます。
いずれにしても、命に関わるのは、喉頭が腫れて気道が閉塞し、低酸素症となって起こるショックです。低酸素によるショックには酸素が必要です。いくら昇圧剤を使っても無効です。十分に心得ておいてください。この点、ガイドラインは不十分です。
アナフィラキシーの症状を起こしているのはマスト細胞の活性化です。出てきたヒスタミンによって下がった血圧を上げようとしても、次々にマスト細胞からヒスタミンが出てきます。だから、「元」を断たなければアナフィラキシーは治まりません。
脱顆粒などを起こすマスト細胞の活性化を断つにはどうすればよいのか。
マスト細胞の脱顆粒など活性化を抑制する主体は、アドレナリンβ2作用とステロイドです。マスト細胞の表面に、どちらの受容体も存在しています。
アドレナリンは、そのβ2受容体に作用して、秒単位でマスト細胞の活性化・脱顆粒を抑制します[16-18]。脱顆粒でヒスタミンの放出を抑制するだけでなく、ロイコトリエンやプロスタグランジンの産生と放出も抑制します[16,18]。
また、ステロイドもマスト細胞の表面の受容体に作用して秒単位、分単位で作用するとともに、マスト細胞内の核内遺伝子に作用して30分から時間単位でマスト細胞の活性化を抑制します[19,20]。。
だから、アナフィラキシー治療には、アドレナリンはもちろん必須ですが、それだけでなく、ステロイドも即座に使っておく必要があるのです。
ガイドライン[5,7,8]には、この「元を絶つ」という考え方が、基本的に希薄です。

「元を絶つ」ためのアドレナリンβ2作用が重要なことは、次の点からも言えます。アドレナリンとノルアドレナリンのα作用(末梢血管収縮作用)およびβ1作用(心収縮力増強)はほぼ同じですから、アドレナリンのα作用(末梢血管の収縮)とβ1作用(心臓の収縮を強化)が重要なら、ノルアドレナリンもアナフィラキシーに効くはずです。しかし実際は全く無効です。だからノルアドレナリンにはないβ2作用こそが重要であることが明瞭です(図2)。
この点についても、日本のアナフィラキシーガイドライン[5,6] は、書き方が極めてあいまいです。
マスト細胞による脱顆粒が進んだ状況では、循環状態をほとんど改善しない[21-24]ということも、「元を絶つ」ことの重要性を示しています。
アナフィラキシーで死亡の原因となるのは、もともとの反応が数分以内に起こるなど超重篤例であることと、アドレナリンの注射時期を失することが極めて重要です[22-24]。脱顆粒などを起こすマスト細胞の活性化を断つにはどうすればよいのか。
たとえば、アナフィラキシーの初期に、血圧が下がっていないからと、アドレナリンの注射をためらっていると、みるみるうちに血圧が下がり、呼吸停止することがあります。
アナフィラキシーによる死亡例では62%でアドレナリンが使用されていましたが、心停止前に使用されていたのは14%に過ぎなかったとの報告があります[23,24]。このほかにもアドレナリンの遅れが死亡につながったことを示唆する調査が何件か報告されています[24]。
ガイドラインのもう一つの欠陥は、ステロイド剤に関する扱いの低さです。日本のガイドライン[5]では「作用発現に数時間を要し、二相性アナフィラキシーを予防する可能性があるが、その効果は立証されていない」、WAOのガイドライン[7]では、「ステロイド剤は、アナフィラキシーにおける持続症状(特に喘息患者)の予防や、二相性反応の予防を目的としてよく用いられているが、アナフィラキシーの急性管理に有益ではない、有害でさえあるかもしれないという証拠が増えてきており、日常的な使用は、議論となってきている。」と記載しています。
しかし、ステロイドがマスト細胞の受容体に結合し、核内遺伝子に作用して炎症誘発物質を抑制するまでの時間は数時間ではなく、早ければ30分程度です[19]。しかも、マスト細胞表面の受容体(遺伝子以外)にも作用して秒単位、分単位で脱顆粒を抑制する作用も有しています[19,20]。
さらに、アドレナリンのβ2受容体に対する耐性[16,25,26] のためにアドレナリンの作用が減弱する1~2時間後にステロイドの効果が強くなってくるので重要です(註2)。人の体内ではこれが自然の仕組みとして働きます。しかし、アナフィラキシーという特別の外的刺激に対しては、アドレナリンとステロイドが適切に作用するように使っておかなければいけません。
日本のガイドライン[5,7]だけでなく、世界アレルギー機関(WAO)のガイドライン[7]でもステロイドの位置づけは高くありません。しかし、WAOが引用したレビュー論文[27]を、詳細に点検したところ、ステロイドは無意味と結論付けていた論文のデータ[28]は、むしろステロイドが再重症化を防いでいたことを如実に示していました。
発症から8時間以上入院を要したアナフィラキシーはきわめて重篤なアナフィラキシーで、240人中ステロイドを使用していなかったのは1人だけでした。したがって、重症化の要因はステロイド以外だったと考えられます(もともと重篤であったことが重要でしょう)。
一方、8時間未満で退院した(比較的軽症と考えられる)アナフィラキシー292人中、ステロイドが使われていた277人(95%)では、再重症化は8人(3%)だけでしたが、ステロイドを使っていなかった15人(5%)では4人(27%)が再重症化していました。ステロイド不使用による再重症化の危険度は12倍でした(図3)[28]
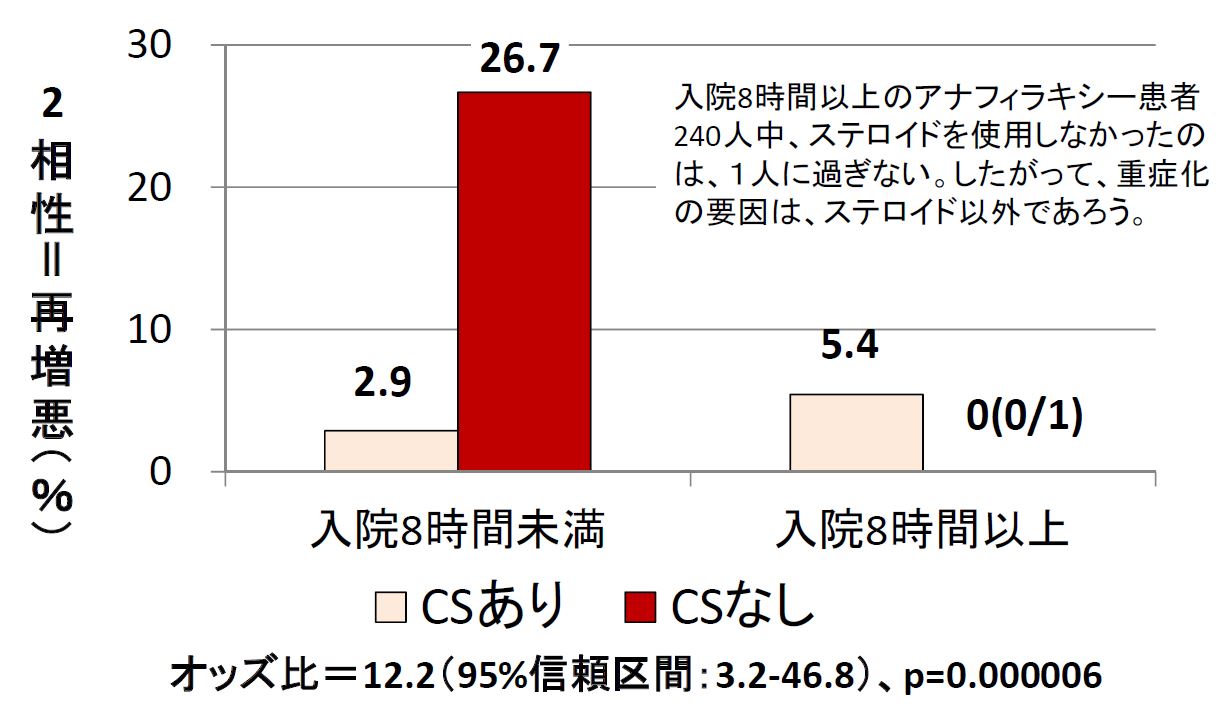
β遮断剤を用いている人における難治性アナフィラキシーで、グルカゴンが推奨されています[5-8]。しかし、世界的に認知されつつあるこの方法は、わずか1例ずつ2件の症例報告[29,30]が根拠です。このほか、日本語の文献も含めてもう1例ずつ[14,31]、合計4件の症例報告が検出できました。
それらを詳細に検討したところ、4例ともすべて、β遮断剤は心選択制、すなわちβ1選択性のβ遮断剤でした。アテノロール2例[29,30]、ビソプロロール1例[14]、メトプロロール1例[31]です。これらβ遮断剤は、アドレナリンのβ2作用を阻害しませんから、アナフィラキシーで活性化されたマスト細胞のβ2受容体を介してアドレナリンは十分に効果を発揮します。
経過をよく検討すると、全例でアドレナリンの使用が不適切でした。うち3例[14,29,30]は造影剤使用直後に血圧低下し、そのうち1例[14]は2分後に心停止が生じた超劇症例でした。アドレナリンを静注して、一旦は心拍が再開、もしくは血圧が一旦上昇しています。しかし、2例[14,30]は10~15分間にアドレナリンを3アンプル(1mg×3)静脈注射が必要でした。1例[29]は、5分後には昇圧効果が消失したとしています。
アドレナリンの効果持続時間は静注した場合、数分以内と極めて短いため、これら症例では、絶対に持続点滴が必要です(註3[32-35])。ところが、3例とも持続点滴をしていません。2例[14,30]では、ノルアドレナリンやドパミンが持続点滴されただけで(註4[36,37])、再度血圧低下をきたしたためにグルカゴンが使用されたものです。
また、1例[29]では、アドレナリン1mg静注後5~10秒後に血圧は80まで上昇したので、効果はあったのですが5分後に消失したため、効果が短いのはβ遮断剤のためと判断され、すぐにグルカゴンが静注されました。しかしこれも約30分後には無効になったためにグルカゴンを持続点滴して血圧を維持できた、というものでした。アドレナリンを持続点滴なしでは、アナフィラキシーが悪化するのは当然です。
もう1例[31]は、気管支喘息のために、抗インターロイキン-5モノクローナル抗体のメポリズマブを使用後のアナフィラキシーでした。アドレナリン0.3mgを3回筋肉注射し、途中でメチルプレドニゾロン125mgを静注して、ようやく、血圧が186/118、心拍77/分と改善しました。ところが、なおも喉が閉まる感じを訴えたために、グルカゴンが使われたものです。
このメポリズマブは、血中濃度がピークに達するのが静脈注射でも2~3時間、皮下注射なら5日程度かかり、半減期が20日前後と極めて長い(添付文書)。そのため、抗原刺激が引き続き起こり、喉頭の閉塞感が持続するなどアナフィラキシー症状が持続したと考えられます。それに、血圧も心拍もβ遮断剤による影響は全く考えられない値(血圧186/118)でした。アナフィラキシーでした。アドレナリン0.3mgを3回筋肉注射し、途中でメチルプレドニゾロン125mgを静注して、ようやく、血圧が186/118、心拍77/分と改善しました。ところが、なおも喉が閉まる感じを訴えたために、グルカゴンが使われたものです。
結局、β遮断剤の使用のために難治であったという4例は、全例、アドレナリンやステロイドの使い方がよくなかったために難治になっただけで、アドレナリンとステロイド剤を適切に使っていれば(註4)、グルカゴンは全く不要の例ばかりでした。
もう1例[31]は、気管支喘息のために、抗インターロイキン-5モノクローナル抗体のメポリズマブを使用後のアナフィラキシーでした。アドレナリン0.3mgを3回筋肉注射し、途中でメチルプレドニゾロン125mgを静注して、ようやく、血圧が186/118、心拍77/分と改善しました。ところが、なおも喉が閉まる感じを訴えたために、グルカゴンが使われたものです。
もう1例[31]は、気管支喘息のために、抗インターロイキン-5モノクローナル抗体のメポリズマブを使用後のアナフィラキシーでした。アドレナリン0.3mgを3回筋肉注射し、途中でメチルプレドニゾロン125mgを静注して、ようやく、血圧が186/118、心拍77/分と改善しました。ところが、なおも喉が閉まる感じを訴えたために、グルカゴンが使われたものです。
グルカゴンは、アドレナリンとは異なる部位に作用して、細胞内でエネルギーのもとになるc-AMPを増やし、アドレナリン様の作用をし、マスト細胞や血管平滑筋、心筋にも作用します[38]。しかし、β遮断剤過量状態に対しても、基本的な治療剤は、アドレナリンやイソプレナリン、バゾプレッシンであり、グルカゴンは、補助的な意味しかありません[39]。
まして、中毒用量ではない通常量のβ遮断剤、特にβ1選択性のβ遮断剤は、アドレナリンのβ2作用には拮抗しないので、アドレナリンとステロイド剤を適切に使用すれば、グルカゴンは必要がありません。
アドレナリンは以前、ハロペリドールやリスペリドンなどの神経遮断剤(抗精神病剤)と併用禁忌になっていましたが、最近、アナフィラキシーの場合は禁忌でなくなりました[40]。
抗精神病剤の過量中毒・循環虚脱型ショックの際には、アドレナリンは現在も併用禁忌です。実際に症例報告が最近でもあります[41,42]。これは、大量の神経遮断剤がアドレナリンのα作用に拮抗し、さらには、アドレナリンのβ2作用によって筋肉の血管が拡張するために血圧が下がるからです。この場合は、β2作用のないノルアドレナリンを使わなければいけません。
しかし、通常量の抗精神病剤を使っている人がアナフィラキシーになった場合は、ノルアドレナリンは無効です。どうしてもアドレナリンが必要ですし、常用量程度の神経遮断剤ではアドレナリンを使っても逆説的血圧低下はまず起こりません。ただし、気道の閉塞はなくなり、呼吸困難はないのに、血圧の戻りだけがよくない場合には、ノルアドレナリンが必要になる場合もありうるかもしれません。
アナフィラキシーに対する治療の原則を、英国のガイドライン[8,43]を一部修正して表2に示します。。
アナフィラキシーは、薬剤による重篤な害反応です。不適切な治療では救命できない場合がありますが、適切な治療をすれば死亡を回避できます。
アナフィラキシーは、適切に速やかに診断し、直ちにアドレナリンを注射し、引き続きステロイドを忘れずに使用しましょう。
