厚生労働省(厚労省)は、2021年11月12日の審議会で、HPV(ヒトパピローマウイルス)ワクチン(いわゆる「子宮頸がんワクチン」の積極的勧奨の再開が了承されたことを受け、11月26日付で、2022年4月からの積極勧奨の再開を決定しました[1]。
厚労省はその主な理由として、2013年に積極勧奨を中止した後の8年間で、多様な症状はワクチン非接種者でも認められる、との厚生科学研究班(祖父江班)の結果[2]や、ワクチン接種が子宮頸がん減少に寄与しているという英国調査[3]の結果をあげています。
しかし、本誌やTIP誌で詳しく扱ってきたとおり[4-11]、HPVワクチンには大きな害が確実にあり、子宮頚がん減少の確かな証拠はありません。害の証拠を示すとともに、再開の根拠となったデータ[2,3]を検証します。なお、この概要は、「薬のチェック」99号(2022年2月発行)で述べます。
また、この記事は、2021年3月に「性の健康財団」における講演[12]を基本に、厚生科学研究班(祖父江班)の結果[2]と最新の英国おける疫学調査の結果[3]についても追加してコメントしたものです。
25歳未満を対象にしたHPVワクチンのランダム化比較試験(RCT)では、有害事象にも、死亡率にも対照群と比較して差がありませんでした[4a,5a,5b]。これ対象者の年齢が若いこと、対照群として、毒性のあるアルミアジュバント(ガーダシルのRCTで)またはアルミアジュバント入りのA型肝炎ワクチン(サーバリックスのRCTで)を使っていることが大きく関係しています。
ところが、25歳~40歳の女性を対象にしたHPVワクチンのRCT3件(4報告[13-16])の総合解析の結果では、総死亡の危険度が対照群に比しオッズ比で5.0倍でした(p=0.002)[17](図1)。これは、ワクチンに強い毒性があることを明瞭に示しています。
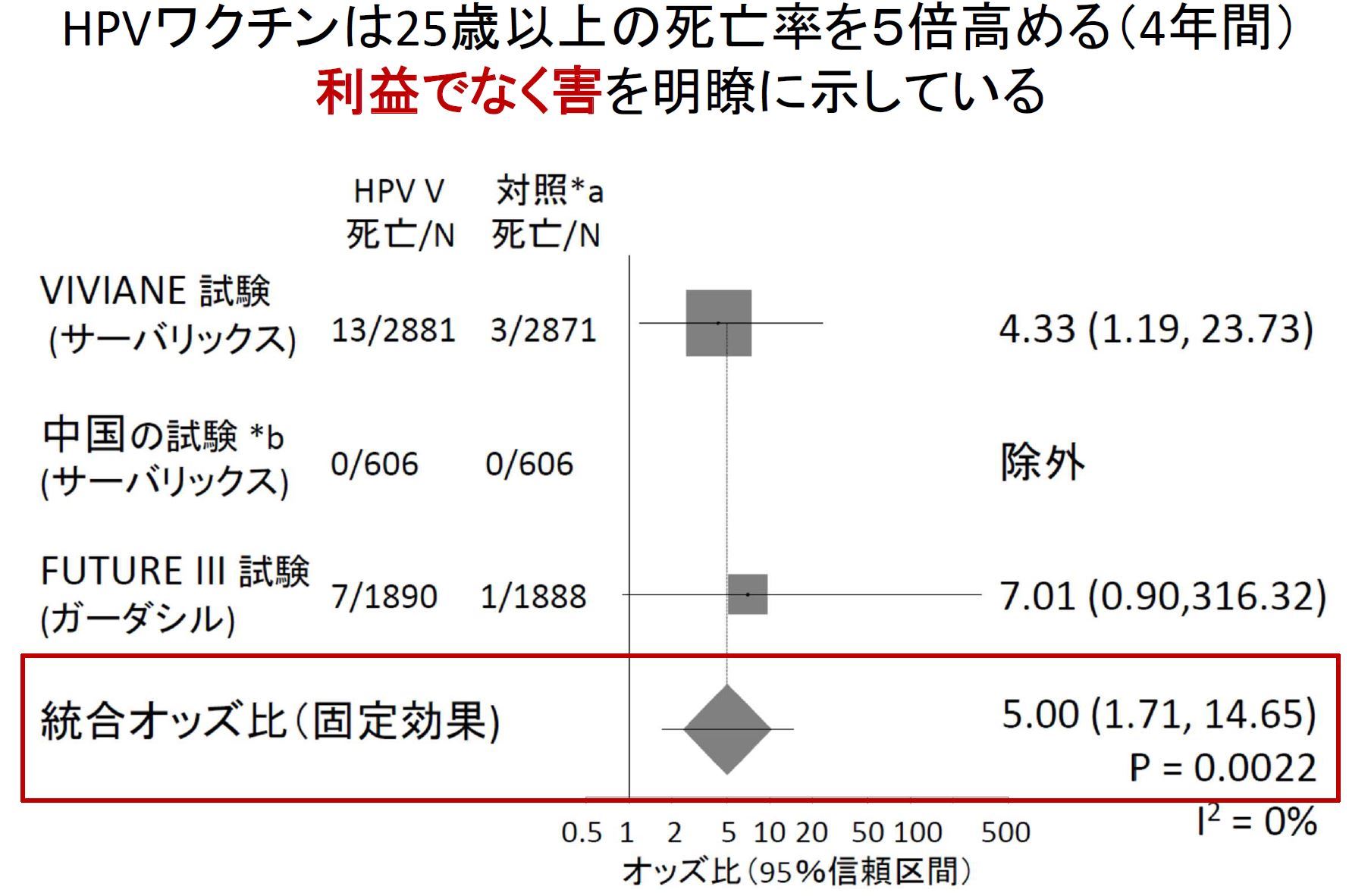
*a: VIVIANE試験(サーバリックス)[13,14]とFUTURE III試験(ガーダシル)[15]ではアラムアジュバント、 中国試験(サーバリックス)[16]ではアラムアジュバント入りB型肝炎ワクチンが対照群に用いられた。
*b:中国試験の追跡期間は1年、他は4年間。
性の健康医学財団の講演会では、触れませんでしたが、厚労省がHPVワクチン積極勧奨再開の重要な根拠の一つとしている厚生科学研究(祖父江班)の結果[2]について、コメントしておきましょう。
これは、2016年度の「子宮頸がんワクチンの有効性と安全性の評価に関する疫学研究」(代表:祖父江友孝)と題する厚生科学研究で、2017年3月に発表されたものです。
このなかで、「12~18 歳における「HPV ワクチン接種後に生じたとされる症状と同様の多様な症状」の有訴率(註:症状を有する人の割合:有症状割合)は、(中略) 女子では人口10 万人あたり40.3、HPV ワクチン接種歴のない女子で人口10 万人あたり20.4と推計された。すなわち、HPV ワクチン接種歴のない青少年においても、「多様な症状」を有する者が一定数存在した。」とまとめられています。
「HPV ワクチン接種後に生じたとされる症状と同様の多様な症状」とは、「広範な疼痛や運動障害等」を指します。これが、厚労省が「多様な症状はワクチン非接種者でも認められる」とした理由になっています。
多様な症状を有するとされた女性1590人中、4割近い604人のワクチン接種状況が不明のため、HPVワクチンの接種歴が明瞭な女性の有症状割合は人口10 万人あたり27.8人でした。ここで、研究班も厚労省も触れていませんが非常に重要なデータを紹介しておきます。
それは、HPV ワクチン接種歴のある女性のうち、接種前に症状のあった人は、人口10 万人あたり1.0人に過ぎないことです(図2)。
これは、接種歴のない人の有症状割合(人口10 万人あたり20.4人)の20分の1にすぎません。接種前や接種後の観察期間、非接種者の観察期間が不明ですので、正確な罹患率の比較ができません。しかし、有症状割合(人口10万人あたり)が接種群では、接種前の1.0から接種後に27.8に大きく変化しています。
一方、接種歴にない人は、接種者のように、接種の前後で著しく有症状者の割合が変化するとは考え難く(年齢により多少の変化はあっても)、若い時期の数年間ではほぼ一定のはずです。12~18歳の期間の半分で有症状者の割合が同じであったとすると、前半(接種者の接種前に相当)では、10万人あたり10.2人となり、これを基準にすると、接種者の接種前の有症状割合はその10分の1にすぎません。
なお、症状が起こった時期が接種前か後かいずれか不明の人が人口10 万人あたり4.0人いました。これらがすべて接種前であったとしても,接種前に症状があった人は、10万人あたり5人にすぎず、接種歴のない女性(人口10 万人あたり20.4人)の4分の1にすぎません。人口10万人あたり4人を、27.8人と1人で比例配分すると接種者の接種前の有症状割合は人口10万人あたり1.14人となります。非接種群の前半の有症状割合10.2人の約9分の1です。
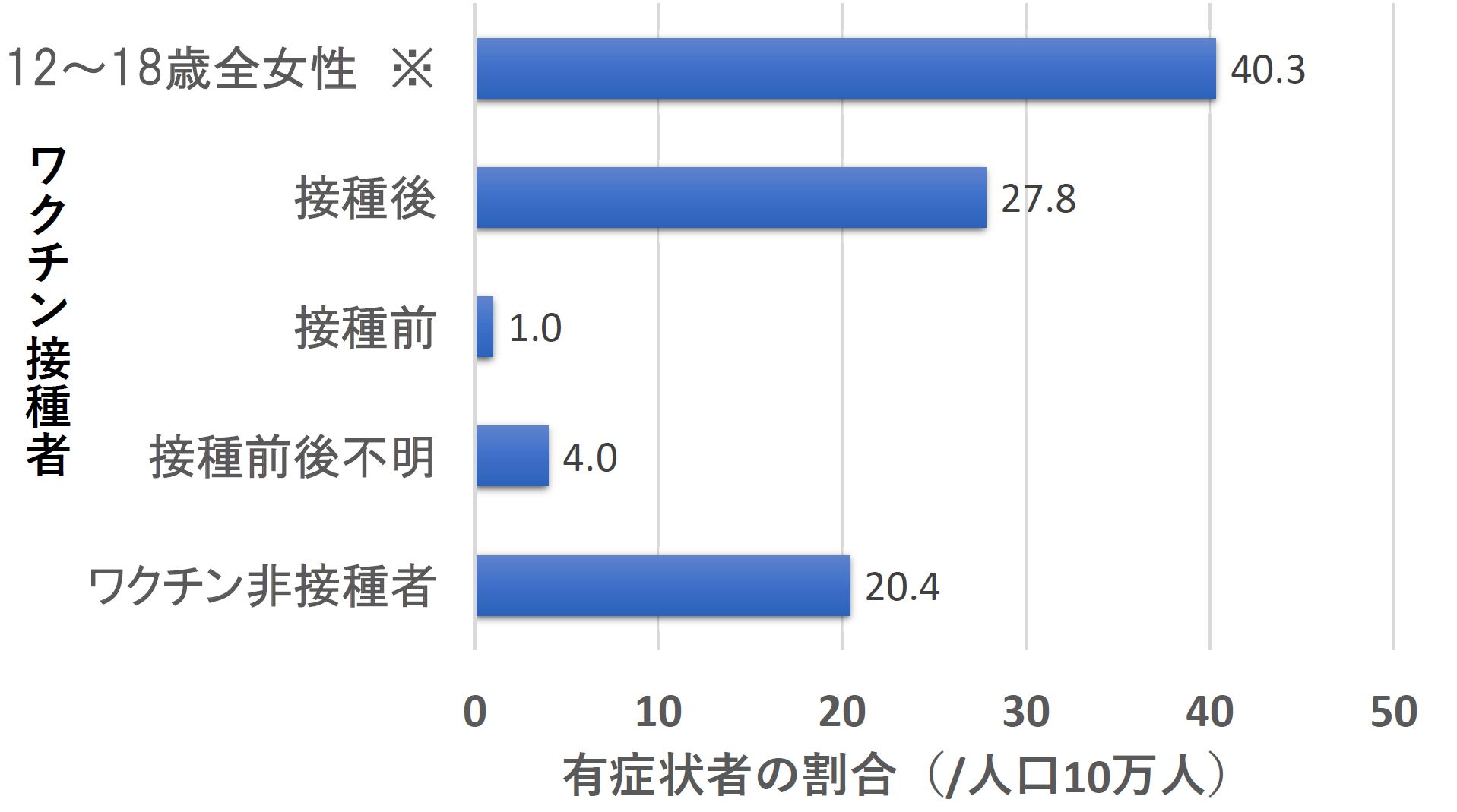
ワクチン接種者の接種前の有症状割合に比べて、非接種群が20倍、接種群は接種後に27.8倍になっている点に注目。
※:多様な症状のある1590人中ワクチン接種の有無が不明の人が604人(38%)おり、非接種者477人や接種者525人よりも多いために12~18歳の全女性中の割合は、接種後の有症状者の割合よりも大きくなっている
これらのことから、HPVワクチンの接種者はもともと、非接種者に比べていかに健康であったかがわかります。そして、HPVワクチンの接種を避けて非接種群となった女性にいかに有症状者が多くなったかが示されているでしょう。
そこで1つでも症状のある人の接種後の危険度1.36倍を、接種前の健康状態で補正する(9.0倍する)と、HPVワクチンによる症状発症の危険度は、約12倍と非常に大きい危険度となります。
さらに、上記の有症状者割合は、症状が1つでもある人の割合です。HPVワクチン接種によるリスク比は27.8/20.4=1.36倍です。ところがこのリスク比は、症状の数が増えるにしたがって大きくなります。症状が10以上ある人の10万人中の割合は、非接種者が5.3人に対して、HPVワクチン接種者は15.6人でした。リスク比は約3倍(15.6/5.3)になっていました。
これらの結果は、次に述べる名古屋調査の結果とよく似ています。
これは、接種歴のない人の有症状割合(人口10 万人あたり20.4人)の20分の1にすぎません。接種前や接種後の観察期間、非接種者の観察期間が不明ですので、正確な罹患率の比較ができません。しかし、有症状割合(人口10万人あたり)が接種群では、接種前の1.0から接種後に27.8に大きく変化しています。
名古屋調査は、15~21歳の女性約7万人を対象にしてHPVワクチン接種前後の症状を調べた大規模なアンケート調査です。その結果は、本誌ですでに報告しました[11f, 11g]。
今回新たに報告したことは、ワクチン接種後の危険度を接種前の症状の危険度で補正し、調整オッズ比とその95%信頼区間を計算で求めたものです。
図3は、接種群で接種前に症状がある程度を、同じ時期の非接種群の有症状の程度と比べて、ロジスティック回帰という方法で危険度(オッズ比)を求めたものです。オッズ比(■)が1(赤縦線|)より少なければ、接種群に症状のある人が少なく、横に伸びた線の右端または左端が1に届いていなければ、統計学的に有意といえます。
ほとんどの症状が、1よりも左にある(少ない)ので、非接種群にくらべて接種群の女性は、接種前には、症状のあった人が少ない。つまり、もともときわめて健康であったといえます。したがって、もともとの健康状態を補正しない限り、接種後に不都合があったとしても、相当高頻度に不都合なことが起こらない限り有意に多くはならないでしょう。接種前の症状の危険度による補正が必要なのはこのためです。
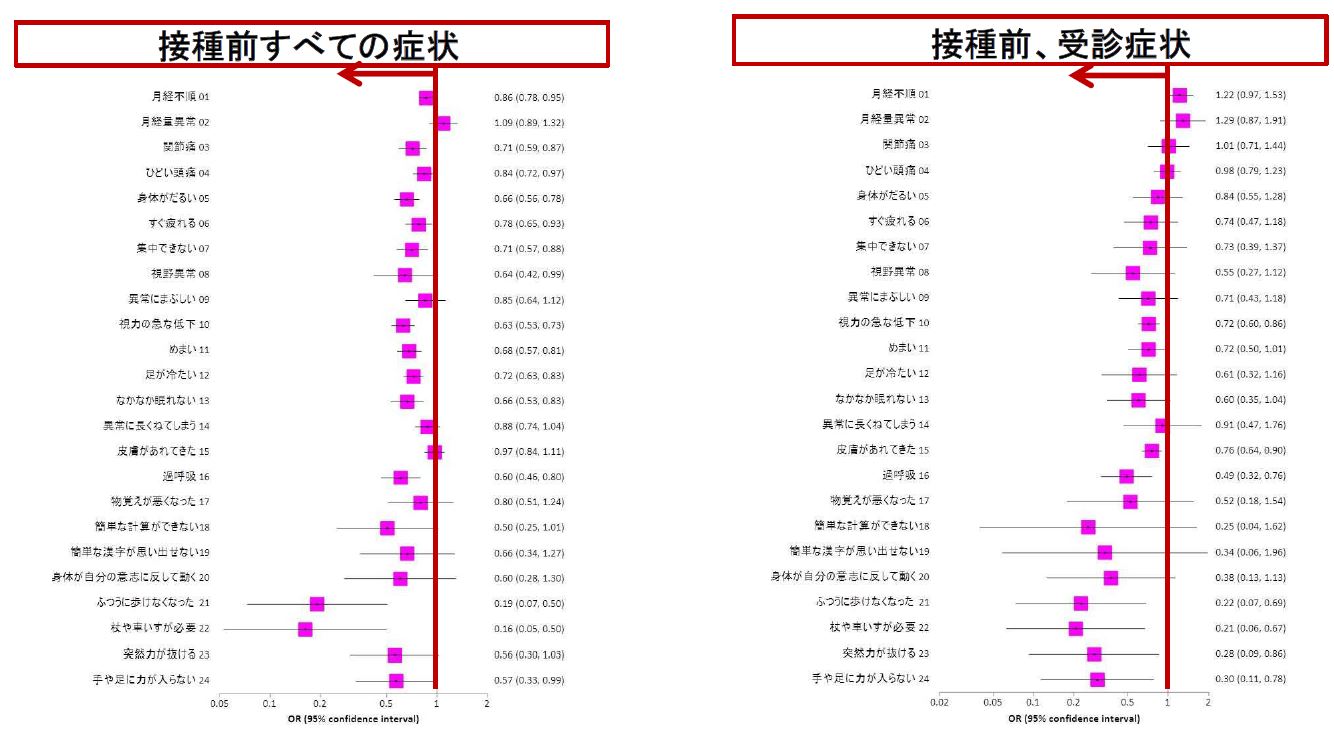
ほとんどの症状が、非接種群に比較してワクチン群で少ない。つまり、ワクチン群はもともと健康な女性が多く、非ワクチン群の女性は病気がちの人が多いことを示している。
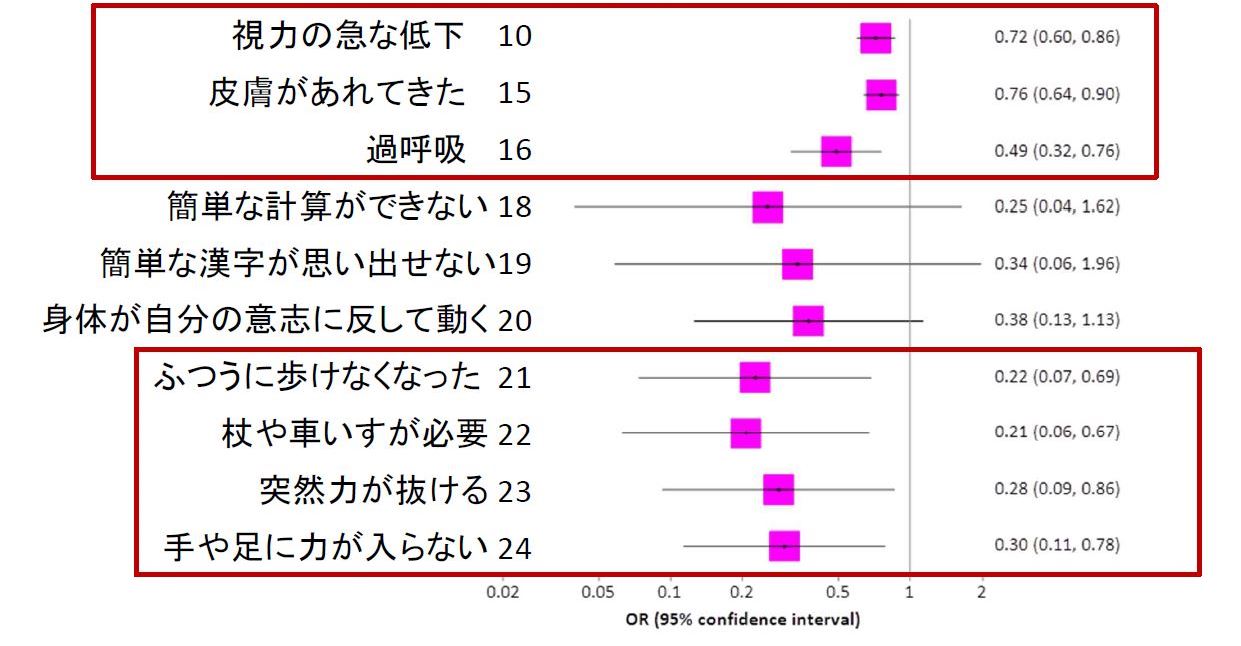
年齢調整ロジスティック回帰分析による。多くの症状、特に重い症状で、接種群が非接種群よりも接種前受診症状が有意に少ない。
図3は文字が小さくて読みづらいので、図4に、接種前に受診する至った主な症状の危険度(非接種群に対する接種群のオッズ比)とその95%信頼区間を示します。接種前には、以下のような症状で受診した人が、非接種群に比べて有意に少ないという結果になりました。
視力の急な低下(オッズ比0.72)、皮膚があれてきた(0.75)、過呼吸(0.49)、普通に歩けなくなった(0.22)、杖や車いすが必要になった(0.21)、突然力が抜ける(0.28)、手や足に力が入らない(0.30)などによる受診です。特に、普通に歩けなくなった、杖や車いすが必要になった、突然力が抜ける、手や足に力が入らないなど、重い症状で受診したことのある人が、接種群に少なく、非接種群にきわめて多く、3~5倍もいたことが特筆すべきことといえるでしょう。
接種後では、受診するに至るような症状は、ほとんどの症状で非接種群よりも接種群で多くなっています。図5に、そのうち主な症状について危険度(非接種群に対する接種群のオッズ比)とその95%信頼区間を示します。
とくに、杖や車いすが必要になって受診した人が非接種群の9.6倍、手や足に力が入らないとの症状で受診した人が非接種群の2.8倍いました。これら重い症状で受診した人は統計学的に有意でした。この2つの接種後に受診した症状が、接種前の症状で補正をしなくとも統計学的に有意であったことは、やはり注目すべきでしょう。
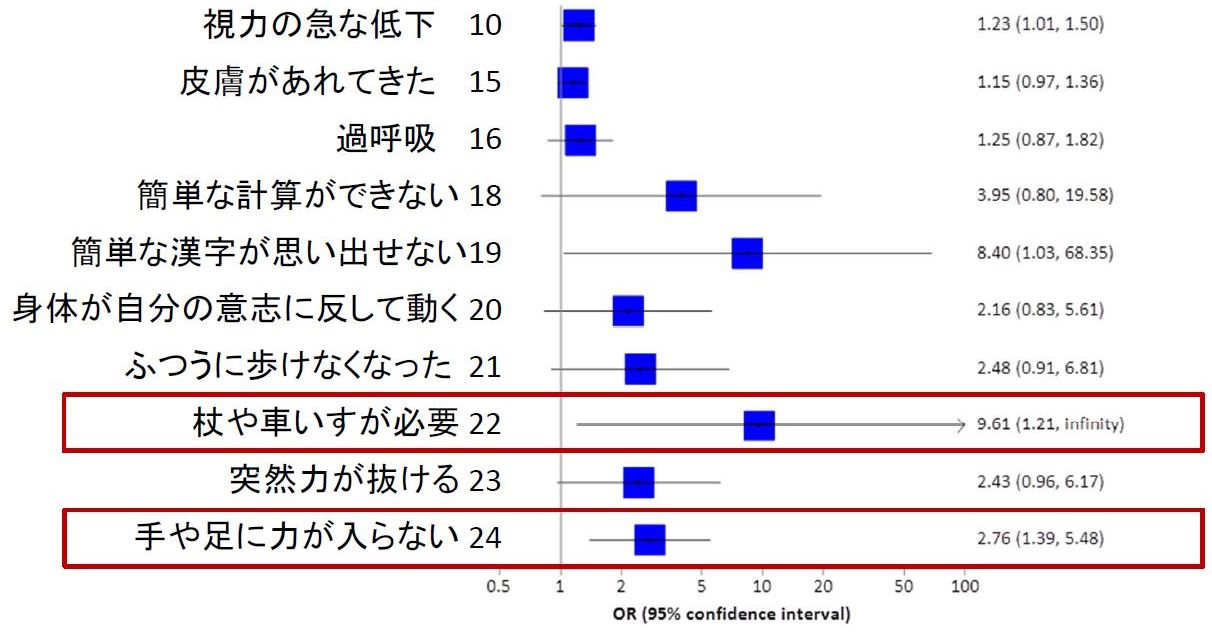
接種前症状の危険度で調整しなくとも「杖や車いすが必要」などは有意に高い。
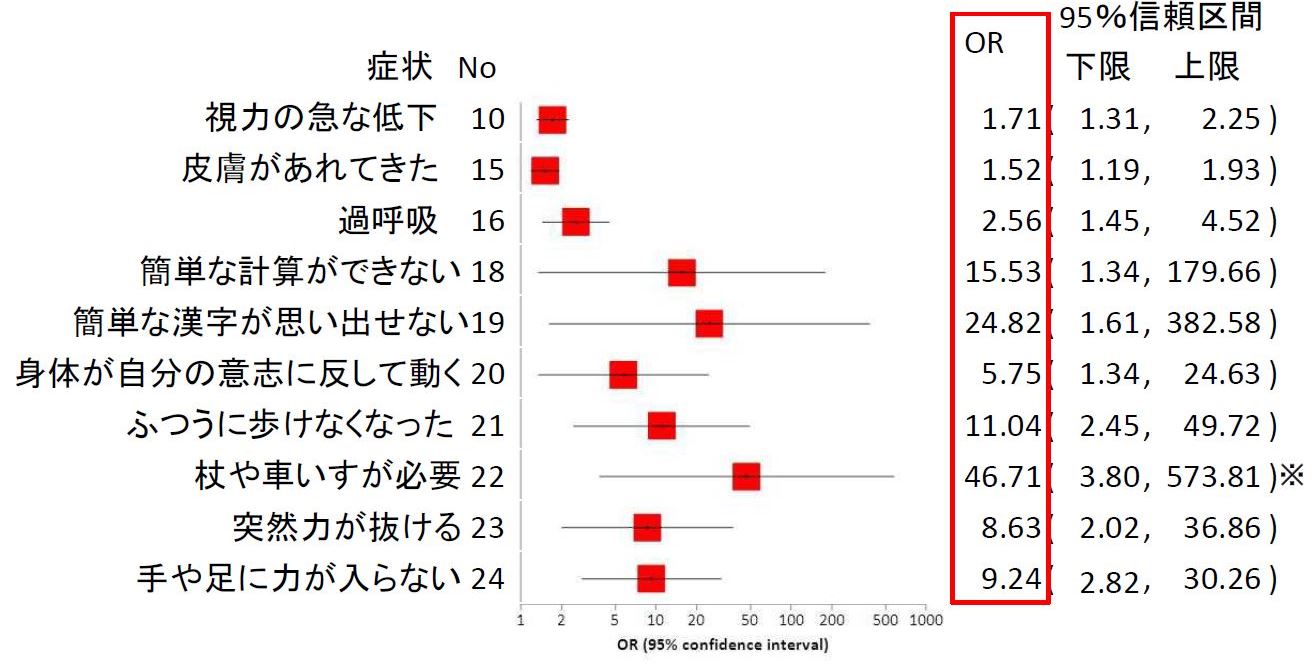
接種前症状で調整すると、極めて大きいオッズ比(OR)になる。OR(オッズ比)とその95%信頼区間は正確である。
ただし、※の95%信頼区間は、接種後受診オッズ比の95%信頼区間上限(∞)を仮に100として計算した値。
接種前の危険度で、接種後の危険度を補正する方法を用いると、接種後に杖や車イスが必要になった人は非接種者に比べて約47倍危険、という結果になりました。
その他、簡単な漢字が思い出せない25倍、簡単な計算ができない16倍、普通に歩けない11倍、手や足に力が入らない9.2倍、突然力が抜ける8.6倍、体が勝手に動く5.8倍などであり、いずれも統計学的に有意でした[12]。
次に、HPVワクチンが子宮頸がんの発症を減少させた、という疫学調査の結果の結果について検討しましょう。これら疫学調査は、厚労省が最も重視した英国の調査[3]のほか、フィンランド[18]と、スウェーデン[19]の調査があります。
フィンランドの調査[18]では、HPV(ヒトパピローマウイルス)と関連のないがん罹患率は、HPVワクチン接種群と非接種群とで差がなかったが、子宮頸がんなどHPV関連がんが有意に少なかった、と報告されました。
しかし有意でないのは、乳がんや甲状腺がんなどHPVと関連のないがんを個々に比較すると、数が少ないためでした。HPV非関連がん全体で比較すると、HPVワクチン非接種群に比較して接種群が0.43倍と有意に少なかったのです(オッズ比0.43、95%信頼区間:0.20-0.93、p=0.028)。
乳がんや甲状腺がんなどHPV非関連がんをHPVワクチンが少なくするはずがないので、接種しなかった人はHPVワクチンの接種を控える何らかの健康問題を抱えていて、それが、がんができやすいことと関係していたと考える必要があります。
何らかの健康問題は、子宮頸がんの発症にも影響するでしょう。そこで、HPVワクチン非接種群の子宮頸がん罹患率も0.43倍してHPVワクチン接種群と比較すると、有意の差はなくなりました。
この調査でワクチン接種率が35%と低かったことと、接種群のHPV非関連がんが非接種群の0.43倍であったことから、理論的に、がんになりやすい人の約半数がHPVワクチンの接種を避けたと推定できます。
接種前の危険度で、接種後の危険度を補正する方法を用いると、接種後に杖や車イスが必要になった人は非接種者に比べて約47倍危険、という結果になりました。
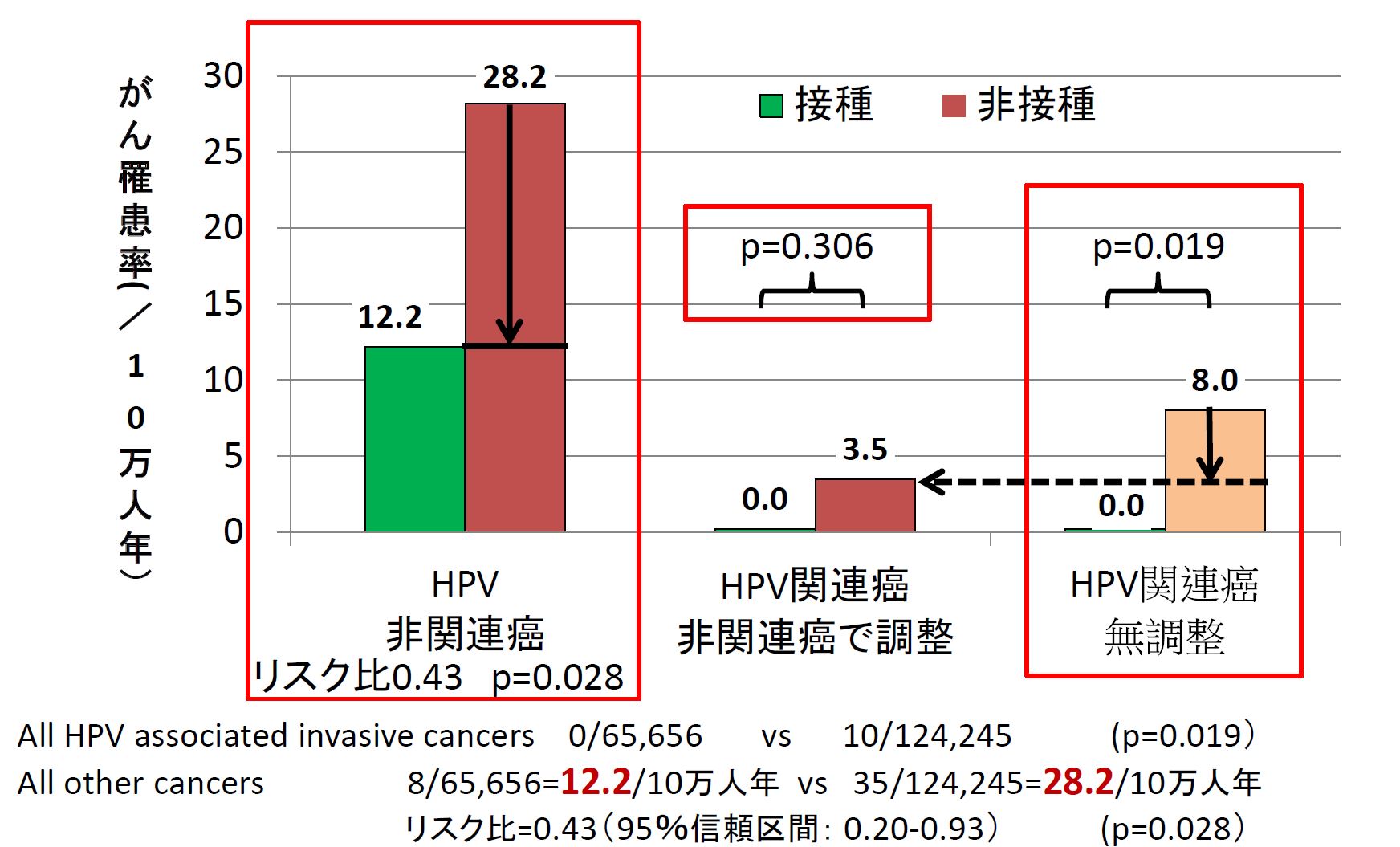
HPVワクチンは他の癌は抑制しないから、この減少は、もともと非接種者の「病気がち」を示す。
非接種群の健康状態が接種群と同じなら、HPV関連癌は10×0.43=4.3人のはず。
0/65,656 vs 4.3/124,245 で比較するとp=0.3057と有意でなくなる。
スウェーデンの調査[19]では、HPVワクチンによる子宮頸がん罹患の危険度は、全年齢で、ワクチンを接種しなかった場合の0.37倍と報告されています。
図8は論文に出ていた図「17歳以上で接種した場合と、17歳未満で接種者した場合、それに非接種群」の子宮頸がん累積罹患率に、本来比較すべき、非接種群の累積罹患率曲線を筆者らが追加したものです。これをどのように計算したか、説明しておきます。
スウェーデンのこの調査[19]から、HPVワクチン接種率はフィンランドとほぼ同じで、35%であることがわかります。
そこで、フィンランド調査と同様に、ワクチン非接種群の子宮頸がん罹患率を0.43倍して、これを基準として計算し直します。すると、ワクチン接種群の危険度は非接種群の0.86倍となり、接種群の子宮頸がん罹患危険度は有意でなくなります。
図8に示した太い赤線は非接種群の曲線を0.43倍したものです。17~30歳で接種した人は、これよりも子宮頸がん累積罹患率が高くなる傾向がありました。
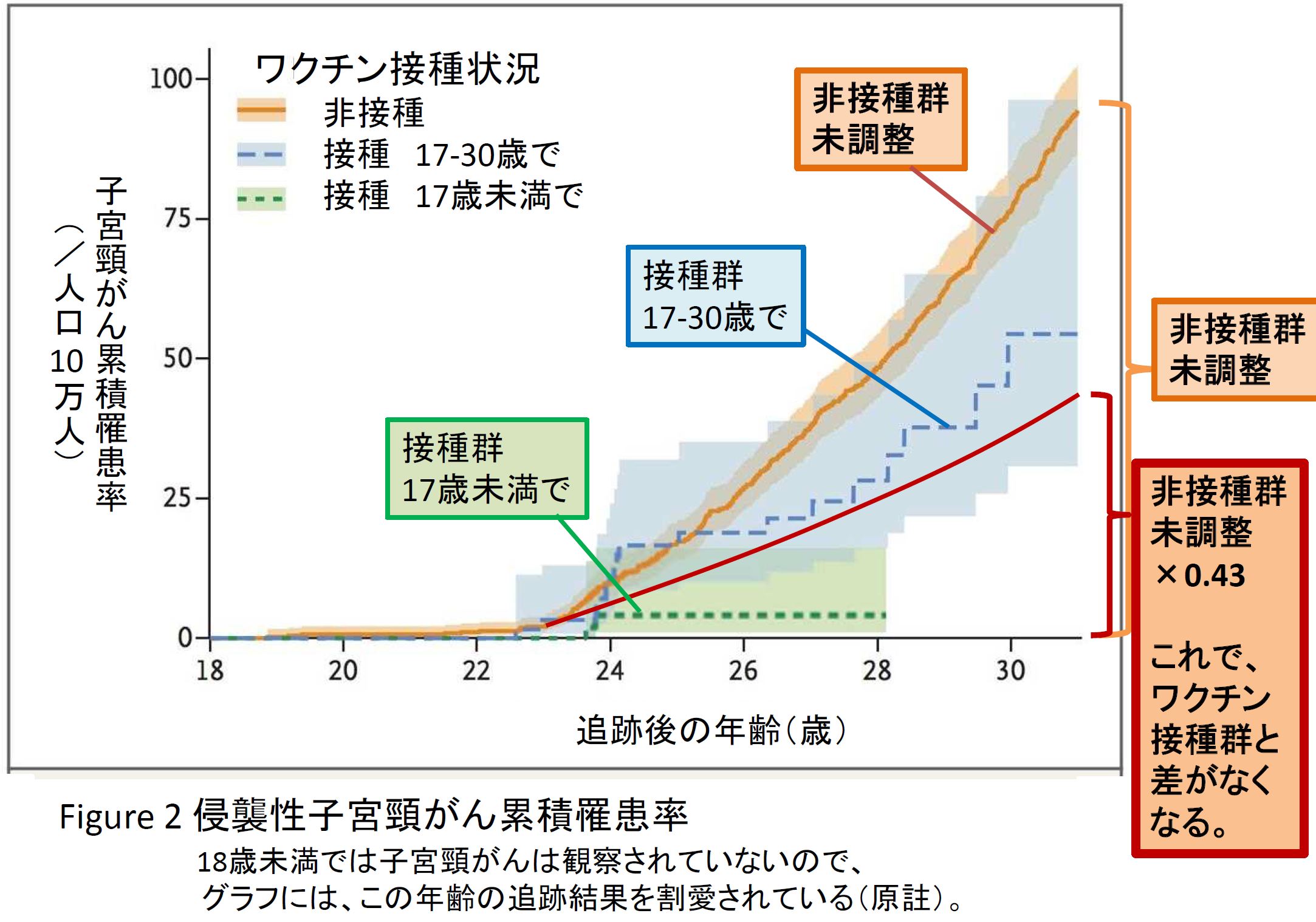
17歳未満で接種した人では、報告された子宮頸がんが2人と少なく、調整リスク比が0.12、95%信頼区間の上限は0.34と報告されています。そのため、フィンランドでの非HPV関連がんのリスク比0.43(95%信頼区間:0.20-0.93)とそれほど差はなく、本当にこの年齢でHPVワクチンの接種を受けると子宮頸がんが予防できるのかどうか、まだ確かなエビデンスとはいえないでしょう。
HPVワクチンの接種率が高い英国で、接種が始まる前の世代(前世代)の人との比較が実施されました[3]。16~17歳にHPVワクチンが接種された女性では、前世代の女性に比べて、子宮頸がんの発生率比が0.66(95%信頼区間:0.59-0.75)、14~15歳に接種した場合は0.38(95%信頼区間:0.29-0.48)、12~13歳の接種ではで0.13(0.06-0.28)で、いずれも有意であったと報告されています。
すなわち、16~17歳に接種すると、その後、子宮頸がんが約3分の2(66%)に、14~15歳の接種で38%に、12~13歳の接種では13%に減少したというのです。
この半数が接種を避ける行為は、ワクチン接種者と同じ時期にワクチンを接種しなかった集団には影響しますが、ワクチン非接種群として、ワクチンを接種していなかった前世代の人には影響がありません。
しかし、健康に問題があるためにワクチン接種を避けた人がいる分、ワクチン接種者中の病気勝ちの人は少なくなっています。したがって、対照群として、接種が始まる前の世代(前世代)の人を選んだとしても、この影響はなくならないので、英国の調査にも適用することができます。
そうすると、16~17歳で接種した人の発生率比(0.66)は0.5より大きく、非接種群(前世代)と差がなくなります。また、14~15歳に接種した場合でも発生率比の95%信頼区間の上限値は0.48ですから、0.5とほとんど差がありません。したがって、非接種群(前世代)と差があるとは言えません。
12~13歳で接種を受けた女性では発生率比の95%信頼区間の上限値は0.28です。接種除外割合の上限値である70%が接種を避けたとすると接種群の病者の危険度は、非接種群の0.3倍となります。この値(0.3)は、12~13歳で接種を受けた女性の発生率比の95%信頼区間上限値0.28とあまり違いません。したがって、この年齢層の女性の場合でも、正確に接種前の健康状態で補正をすると、非接種群(前世代)と比べて有意の差がでるかどうかは微妙です。
この論文[3]の著者らは、12~13歳で顕著な効果があるとし、その原因として、12~13歳ではHPVに感染していないことが関係するとしています。そうであるならば、14歳になると女性の相当数に性交渉がありHPVに感染しているということになります。果たして本当にそのようなことがあるのか疑問です。
むしろ、この年齢層についても、子宮頸がんの発症を防止しているように見えるのは、単に健康者接種バイアスの影響が強いだけではないかと疑われます。そして、この年齢層では特に健康に問題のある女性が接種を控える傾向が強いということが関係してはいないか、吟味が必要であると考えます。
健康者接種バイアスを無視した観察研究の結果で積極勧奨を再開するのは危険です。